トレンドトピック
#
Bonk Eco continues to show strength amid $USELESS rally
#
Pump.fun to raise $1B token sale, traders speculating on airdrop
#
Boop.Fun leading the way with a new launchpad on Solana.
@NatChemBio年に発表されたCore Investigator @li_lingyinの新しい論文では、マウスモデルで強い活性があるにもかかわらず、ヒトSTING阻害剤の有効性が限定的である理由を調査しています。
@xujun_caoと@rjchan426が主導したこの研究では、STINGの一般的に標的とされる部位がヒトのシグナル伝達に必要ないことを発見し、代替の調節メカニズムを特定しました。

論文へのリンク:
Li氏らは、H-151を含むいくつかの阻害剤化合物の標的であるC91パルミトイル化が、ヒトのSTINGシグナル伝達には不要であることを示しています。
これは、一部の阻害剤がマウス細胞ではSTINGをブロックし、ヒト免疫細胞ではブロックしない理由を説明するのに役立ちます。
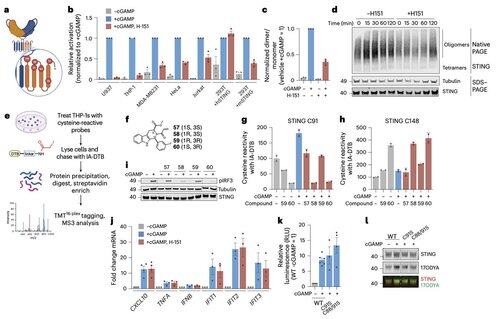
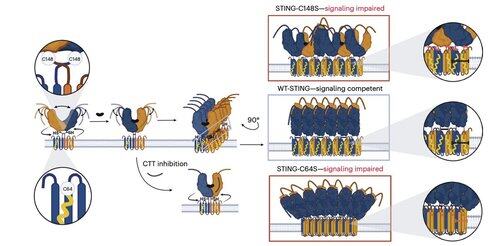
それどころか、Li氏のチームは、保存され、基礎的にパルミトイル化されたシステインであるC64が、ヒトのSTING活性化に不可欠であることを発見しました。
C64は、STINGが非生産的オリゴマーに早期に組み立てられるのを防ぎ、活性化前の重要なチェックポイントとして機能します。
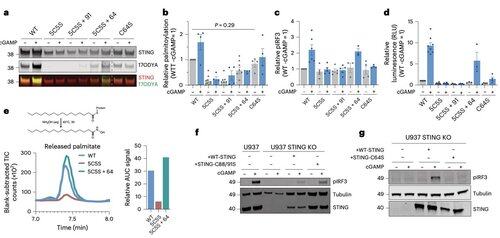
C64およびC91でのパルミトイル化は、C148でのジスルフィド結合を制御し、STINGオリゴマーを安定化させます。
このジスルフィド形成は必要ですが、それが早すぎるとSTINGが不活性状態に閉じ込められてしまいます。
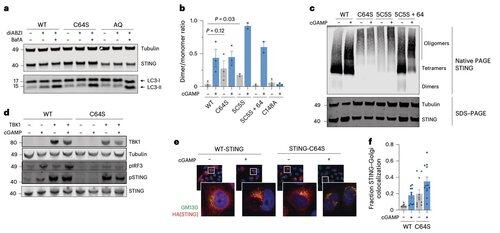
コンテキスト依存的な修飾の限界を超えるために、Li氏のチームはオリゴマー化インターフェース自体に焦点を当てました。
これにより、表面に露出した明確なポケットに結合し、STINGの活性化をブロックする最小限の8アミノ酸ペプチドが発見されました。
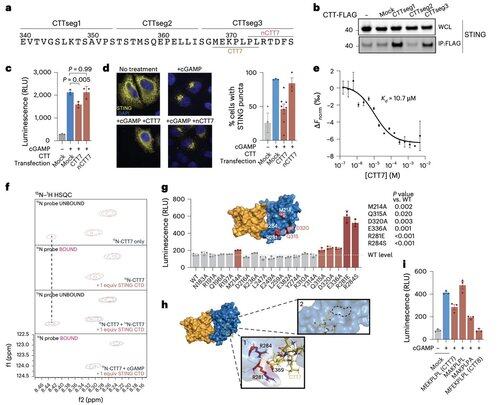
このインターフェースは、これまで認識されていなかったヒトSTING上の薬物アクセス可能な部位を定義し、状況を問わずに有効な阻害剤を設計するための有望な方向性を提供します。これは、自己免疫と炎症における将来の治療法開発の舞台となります。
詳細情報:
6.17K
トップ
ランキング
お気に入り













